Das Hormon Insulin reguliert den Blutzuckerspiegel im Körper. Es regt nicht nur Körperzellen an, Glukose aus dem Blut aufzunehmen, sondern spielt auch bei der Kontrolle des Stoffwechsels durch das Gehirn eine wichtige Rolle. Bei fettleibigen Menschen wirkt das Hormon Insulin – vermutlich auch aufgrund von entzündlichen Prozessen – nicht mehr richtig. Diese Insulinresistenz ist ein wesentliches Kennzeichen für die Entwicklung eines Typ-2-Diabetes. Allerdings sind die Ursachen für eine Insulinresistenz nicht genau geklärt. In neueren genomweiten Assoziationsstudien (GWAS) wurde DUSP8 als ein Risikogen für Typ-2-Diabetes identifiziert. In der aktuellen Studie untersuchten Forschende, welche Rolle das Protein Dusp8 (Dual Specificity Phosphatase 8), das von dem Gen DUSP8 codiert wird, bei der Krankheitsentstehung spielt.
Genetische Variante des Gens DUSP8 erhöht Risiko für Typ-2-Diabetes
„Träger einer genetischen Variante des Gens DUSP8 haben ein erhöhtes Risiko an Typ-2-Diabetes zu erkranken. Bisher weiß man allerdings noch nicht, welche funktionelle Bedeutung das Protein Dusp8 für die Entwicklung der Stoffwechselerkrankung hat“, erklärt Dr. Sonja C. Schriever, Hauptautorin der Studie. „In unseren Untersuchungen analysierten wir zelluläre Modelle, Mäuse mit und ohne Dusp8-Gen sowie funktionelle Magnetresonanztomographien von Menschen mit Varianten des Gens“, berichtet Letztautor Prof. Dr. Paul Pfluger. Im Rahmen des Deutschen Zentrums für Diabetesforschung (DZD) stellten die beiden Forschenden ein Team aus den Bereichen Biologie, Epidemiologie und klinische Medizin auf, das die molekularen Mechanismen entschlüsseln konnte, die das Protein Dusp8 mit der Entstehung von Typ-2-Diabetes in Verbindung bringen. „Wir konnten zeigen, dass es wichtige Weichen für die Wirkung von Insulin im Gehirn und für den Glukosestoffwechsel stellt“, sagt Pfluger.
Protein Dusp8 hat regulatorische Wirkung auf die hypothalamische Insulinsensitivität
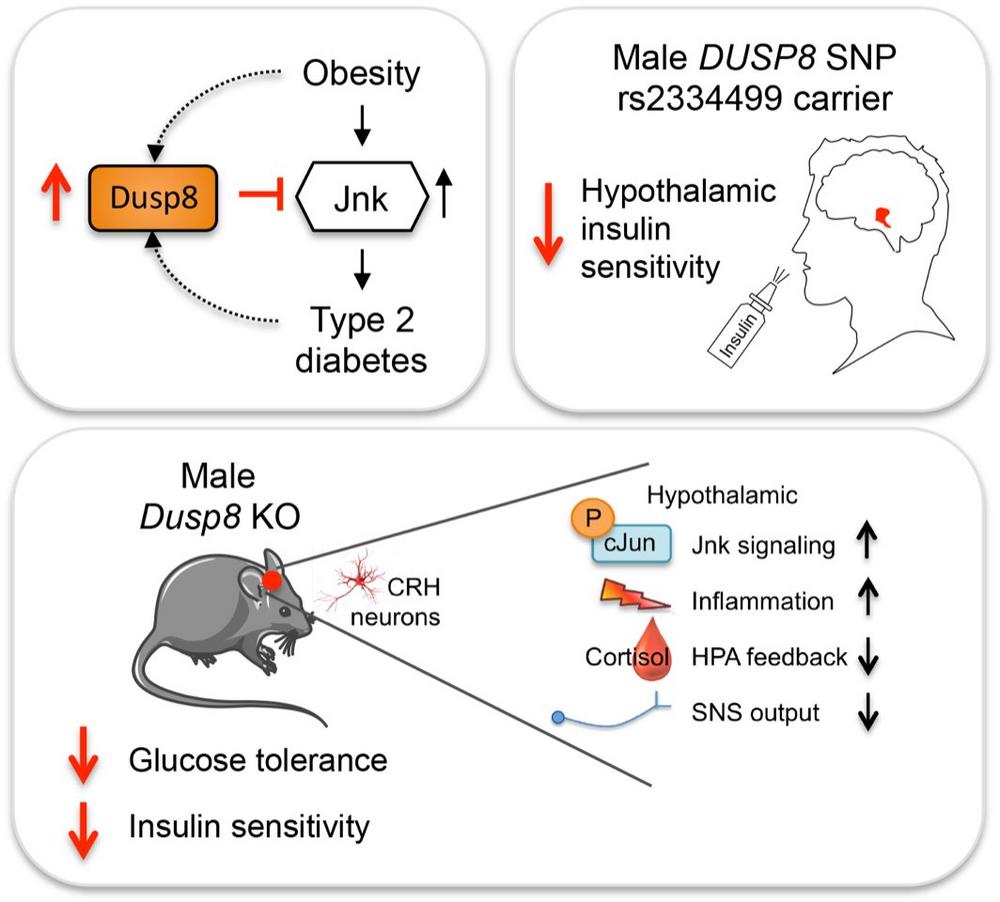
Das Protein Dusp8 hat einen regulatorischen Einfluss auf Entzündungsprozesse im Gehirn im Bereich des Hypothalamus sowie auf den hormonellen Regelkreis zwischen Hypothalamus, Hypophyse und Nebennierenrinde. Es scheint u.a. vor Entzündungsprozessen sowie vor einer verminderten Wirkung des Hormons Insulin im Gehirn zu schützen. Im Tiermodell konnten die Forschenden zeigen, dass bei männlichen aber nicht bei weiblichen Tieren, denen das Gen Dusp8 fehlt und die daher nicht das entsprechende Protein bilden konnten, entzündliche Prozesse zunahmen, der Regelkreis zwischen Hypothalamus, Hypophyse und Nebennierenrinde gestört war, verstärkt Stresshormone gebildet wurden und in Folge dessen die Insulinsensitivität sank. Die geschlechtsspezifische Wirkung des Proteins Dusp8 konnte für den Menschen bestätigt werden, da nur bei Männern, die Träger der Risikovariante des Gens DUSP8 waren, die Insulinsensitivität im Gehirn verringert war.
„Die Aufklärung der multisystemischen Prozesse, welche die Insulinsensitivität im Hypothalamus in den Mausmodellen beeinträchtigen, war ein wichtiger Schritt, um die mechanistischen Grundlagen des Typ-2-Diabetes-Risikogens DUSP8 zu verstehen“, sagt Schriever. In weiteren Studien wollen die Forschenden untersuchen, welche Wirkung Insulin und die Risikovariante des Gens DUSP8 bei menschlichen Probanden mit oder ohne Typ-2-Diabetes auf die Hypothalamus-Hypophysen-Nebennieren-Achse haben.
Original-Publikation:
Schriever SC et. al: Das Typ-2-Diabetes-Risikogen Dusp8 reguliert die hypothalamische Jnk-Signalisierung und die Insulinsensitivität. J Clin Invest. 2020 Aug 11:136363. doi: 10.1172/JCI136363. PMID: 32780722.
Die Research Unit NeuroBiology of Diabetes (NBD) am Helmholtz Zentrum München, ist mit dem Institut für Diabetes und Adipositas (IDO) assoziiert und Teil des HDC und DZD. NBD untersucht die Rolle des Zentralnervensystems (ZNS) als möglichen gemeinsamen Nenner für Adipositas und Typ-2-Diabetes. Weitere Schwerpunkte der Forschungsabteilung sind die molekularen Grundlagen für Leptinresistenz und epigenetische Vorgänge in der Gewichtsregulation. www.helmholtz-muenchen.de/nbd
Das Helmholtz Zentrum München verfolgt als Forschungszentrum die Mission, personalisierte medizinische Lösungen zur Prävention und Therapie von umweltbedingten Krankheiten für eine gesündere Gesellschaft in einer sich schnell verändernden Welt zu entwickeln. Der Hauptsitz des Zentrums liegt in Neuherberg im Norden Münchens. Das Helmholtz Zentrum München beschäftigt rund 2.500 Mitarbeitende und ist Mitglied der Helmholtz-Gemeinschaft, der größten Wissenschaftsorganisation Deutschlands mit mehr als 40.000 Mitarbeitenden in 19 Forschungszentren. www.helmholtz-muenchen.de
Das Deutsche Zentrum für Diabetesforschung (DZD) e.V. ist eines der sechs Deutschen Zentren der Gesundheitsforschung. Es bündelt Experten auf dem Gebiet der Diabetesforschung und verzahnt Grundlagenforschung, Epidemiologie und klinische Anwendung. Ziel des DZD ist es, über einen neuartigen, integrativen Forschungsansatz einen wesentlichen Beitrag zur erfolgreichen, maßgeschneiderten Prävention, Diagnose und Therapie des Diabetes mellitus zu leisten. Mitglieder des Verbunds sind das Helmholtz Zentrum München – Deutsches Forschungszentrum für Gesundheit und Umwelt, das Deutsche Diabetes-Zentrum DDZ in Düsseldorf, das Deutsche Institut für Ernährungsforschung DIfE in Potsdam-Rehbrücke, das Institut für Diabetesforschung und Metabolische Erkrankungen des Helmholtz Zentrum München an der Eberhard-Karls-Universität Tübingen und das Paul-Langerhans-Institut Dresden des Helmholtz Zentrum München am Universitätsklinikum Carl Gustav Carus der TU Dresden, assoziierte Partner an den Universitäten in Heidelberg, Köln, Leipzig, Lübeck und München sowie weitere Projektpartner. www.dzd-ev.de
Deutsches Zentrum für Diabetesforschung e.V.
Ingolstädter Landstrasse 1
85764 Neuherberg
Telefon: +49 (89) 3187-2086
http://www.dzd-ev.de
Helmholtz Zentrum München
Telefon: +49 (89) 3187-2104
E-Mail: paul.pfluger@helmholtz-muenchen.de
Presse- und Öffentlichkeitsarbeit
Telefon: +49 (89) 3187-3971
E-Mail: niesing@dzd-ev.de
![]()